Haimasyöpä löytyy usein liian myöhään. Mayo Clinicin AI-malli löysi siitä merkkejä tavallisista vatsan CT-kuvista mediaanisti noin 16 kuukautta ennen diagnoosia.
Se kuulostaa siltä kuin lääketiede olisi hypännyt eteenpäin yhdellä loikalla. Todellisuus on kiinnostavampi. Malli toimii toisena lukijana hiljaisen datan päällä: se katsoo samaa kuvaa kuin ihminen, mutta eri tavalla.
Uutinen, joka kannattaa ottaa vakavasti
Mayo Clinic julkaisi 29.4.2026 tulokset REDMOD-mallista. Nimi tulee sanoista Radiomics-based Early Detection Model. Käytännössä kyse on kuvantamismallista, joka analysoi tavallisia vatsan CT-kuvia ja etsii kudoksen rakenteesta merkkejä, joita ihminen ei välttämättä huomaa.
Tutkijat ajoivat mallilla lähes 2 000 CT-kuvaa. Mukana oli kuvia potilailta, joilla haimasyöpä diagnosoitiin myöhemmin. Tärkeä yksityiskohta: nämä kuvat oli alun perin tulkittu normaaleiksi. Lääkäri ei siis ollut katsonut kuvaa huolimattomasti. Näkyvää kasvainta ei vielä ollut.
REDMOD tunnisti 73 prosenttia esidiagnostisista syövistä mediaanisti noin 16 kuukautta ennen diagnoosia. Joissain tapauksissa malli löysi signaalin jopa kolme vuotta ennen kliinistä diagnoosia. Yli kaksi vuotta ennen diagnoosia otetuissa kuvissa AI tunnisti lähes kolme kertaa enemmän varhaisia syöpiä kuin pelkkä erikoislääkärien uudelleentarkastus.

Tämä ei vielä tarkoita, että haimasyövän seulonta muuttuu huomenna. Mayo Clinic vie mallia seuraavaksi AI-PACED-nimiseen kliiniseen testaukseen. Siinä arvioidaan muun muassa, miten AI-löydös istuu potilaan hoitopolkuun, paljonko syntyy vääriä positiivisia ja paranevatko kliiniset lopputulokset.
Juuri tämä on olennainen kohta. Terveydenhuollossa mallin näyttävä testitulos on vasta alku. Todellinen kysymys on, mitä tapahtuu, kun tulos viedään vastaanoton, potilastietojärjestelmän, jatkotutkimusten ja lääkärin päätöksenteon keskelle.

Miksi juuri haimasyöpä on hyvä esimerkki
Haimasyöpä on raju esimerkki siksi, että se on usein hiljainen liian pitkään. Mayo Clinic viittaa National Cancer Instituten lukuihin: yli 85 prosenttia potilaista saa diagnoosin vasta, kun tauti on jo levinnyt, ja viiden vuoden elossaololuku jää alle 15 prosenttiin.
Varhainen havainto voi siis muuttaa paljon. Mutta se ei tee asiasta yksinkertaista.
Jos tauti on harvinainen, laajasta seulonnasta syntyy helposti ongelma. Pieni väärien hälytysten osuus voi tarkoittaa suurta määrää turhia jatkotutkimuksia, huolta ja kustannuksia. CT-kuvat eivät ole harmittomia arkikuvia. Ne maksavat, vievät resursseja ja altistavat säteilylle.
Siksi REDMODin kiinnostavin käyttötapa ei välttämättä ole koko väestön seulonta. Se voi olla paljon rajatumpi: korkeamman riskin potilaat ja kuvat, jotka on jo otettu muista syistä. Esimerkiksi Mayo Clinic mainitsee uuden diabeteksen kaltaiset riskitilanteet.
Tässä AI on parhaimmillaan. Se ei pyydä maailmaa muuttamaan itseään mallin ympärille. Se tulee olemassa olevan datavirran päälle ja etsii sieltä signaalin, jonka löytäminen käsin olisi liian hidasta tai epävarmaa.
Potilaan kannalta tästä ei silti seuraa ohjetta tulkita omia oireita tekoälyllä. Jos oireet huolestuttavat, oikea osoite on edelleen terveydenhuollon ammattilainen. Tässä puhutaan kliinisestä työkalusta, ei kotikäyttöisestä ennustuskoneesta.
Toinen kehityslinja on paljon suurempi kuin diagnoosi
Samana päivänä, 29.4.2026, Biohub julkisti Virtual Biology Initiative -hankkeen. Viiden vuoden panostus on 500 miljoonaa dollaria.
Tämä uutinen on vähemmän potilasläheinen, mutta pitkällä aikavälillä ehkä vielä isompi. Biohub haluaa rakentaa avoimen data- ja mittauspohjan AI-kiihdytetylle biologialle. Tavoitteena on ennustava malli solusta: järjestelmä, jolla tutkija voisi kysyä, mitä solussa tapahtuu, jos tiettyä mekanismia muutetaan.
Ajatus on helppo sanoa ja vaikea toteuttaa. Solu on dynaaminen järjestelmä, jossa molekyylit, proteiinit, geenit, kudokset ja ympäristö vaikuttavat toisiinsa jatkuvasti. Kaukana Excel-taulukosta.
Biohubin oma selitys on selvä: nykyinen data ei riitä. Tarvitaan kertaluokkia enemmän multimodaalista biologista dataa, parempia mittausmenetelmiä ja suurta laskentakapasiteettia. Hankkeessa on mukana muun muassa Allen Institute, Arc Institute, Broad Institute, Wellcome Sanger Institute, Human Cell Atlas ja Human Protein Atlas. NVIDIA tukee laskentainfrastruktuurissa.
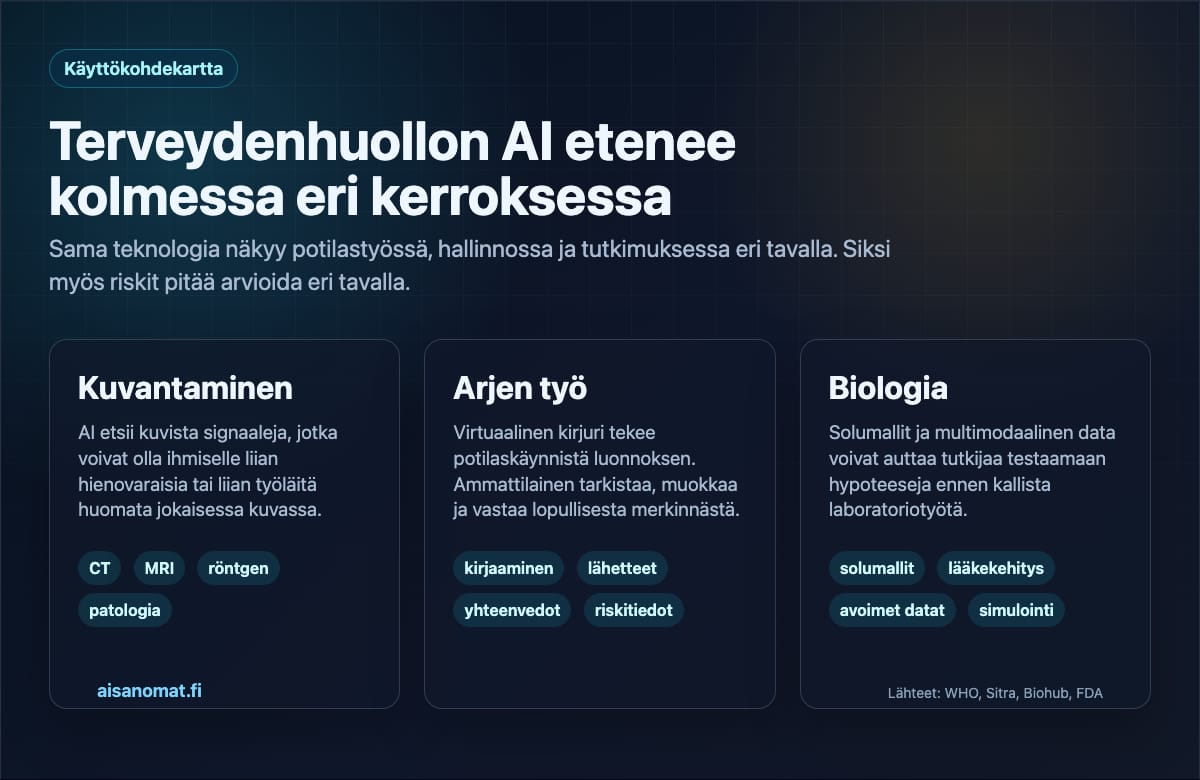
Tämä jakaa terveydenhuollon AI:n kahteen eri aikajänteeseen.
Ensimmäinen on kliininen arki. Siinä AI lukee kuvia, laatii potilaskirjausten luonnoksia, nostaa riskisignaaleja ja auttaa lääkäriä tekemään päätöksiä paremmalla tiedolla.
Toinen on tutkimus. Siinä AI yrittää lyhentää matkaa hypoteesista kokeeseen. Jos solun käyttäytymistä voi mallintaa riittävän hyvin, tutkija voi testata joitakin ajatuksia digitaalisesti ennen kallista laboratoriotyötä.
Nämä kaksi tasoa etenevät nyt samaan aikaan. Siksi "AI terveydenhuollossa" on liian pieni ilmaus. Kyse on sekä vastaanoton arjen uudistamisesta että biologisen tutkimuksen työkalupakin muuttumisesta.

AI on jo sairaaloissa, mutta epätasaisesti
Tätä ei tarvitse odottaa kymmenen vuotta. AI on jo terveydenhuollossa.
FDA:n oma AI-enabled medical devices -lista sisälsi tätä kirjoittaessa 1 430 laitetta tai ohjelmistoa, joiden päätöspäivät ulottuvat vuoden 2025 loppuun. Lista antaa vain osakuvan markkinasta, mutta se kertoo suunnan: AI on siirtynyt tutkimuspaperien lupauksesta luvitetuksi tuoteryhmäksi.
JAMA Network Open julkaisi keväällä 2025 analyysin 903 FDA:n listalla olleesta AI-laitteesta. Niistä 692 eli 76,6 prosenttia liittyi radiologiaan. Se on loogista. Kuvantamisessa data on rakenteisempaa kuin vapaassa vastaanottokeskustelussa, tulos on helpompi mitata ja työnkulku on usein selkeä.
Kuvantaminen on terveydenhuollon AI:lle vähän sama kuin varastoautomaatio verkkokaupalle. Se on rajattu ympäristö, jossa syöte, tehtävä ja palaute ovat suhteellisen selviä. Kuva tulee järjestelmästä, malli analysoi sen ja ammattilainen näkee löydöksen omassa työkalussaan. Siinä on paljon vähemmän tulkinnanvaraa kuin tilanteessa, jossa potilas kertoo kolmesta oireesta, viidestä lääkkeestä ja kahdesta huolesta saman vastaanoton aikana.
Rajatussa tehtävässä mallin onnistumista voi myös seurata jälkikäteen. Löytyikö löydös? Montako turhaa hälytystä syntyi? Muuttiko tulos hoitoa? Vastaanottokeskustelussa sama mittaaminen on paljon vaikeampaa.
Tämä selittää myös, miksi osa terveydenhuollon AI-keskustelusta menee helposti ohi. Kun puhutaan "AI-lääkäristä", mielikuva on keskusteleva yleismalli, joka antaa diagnoosin. Todellinen käyttöönotto alkaa usein paljon tylsemmästä kohdasta: kuvasta, kirjausluonnoksesta, riskilistasta tai lääkityksen tarkistusvaiheesta. Juuri siksi se on uskottavampaa.
Suomessa kehitys näkyy arkisemmin. Sitra-rahoitteisissa kokeiluissa Pohde, Oma Häme ja Länsi-Uudenmaan hyvinvointialue testasivat AI-avusteista potilaskirjaamista ja muita työtä keventäviä sovelluksia. Oma Hämeen pilotissa lääkärit arvioivat, että AI tuotti noin 80-prosenttisesti valmiin yhteenvedon, jonka lääkäri tarkisti ennen potilastietojärjestelmään viemistä.
Tuo on vähemmän dramaattista kuin syövän löytäminen vuosia etukäteen. Mutta terveydenhuollon arjessa se voi olla valtavan käytännöllistä. Jos lääkäri käyttää jokaisella käynnillä vähemmän aikaa kirjaamiseen, potilaalle jää enemmän huomiota. Jos potilas saa ymmärrettävämmän tekstin OmaKantaan, hoidon jatkuvuus paranee.
Sitra nosti esiin myös rajat. Lyhyissä kokeiluissa tarkkoja aikasäästöjä ei aina ehditty mitata. Mallit eivät tunnistaneet kaikkea erikoissanastoa, ja tietosuojan vaikutustenarviointi vei aikaa. Juuri tällaista terveydenhuollon AI usein on: lupaavaa, käytännöllistä ja hallinnollisesti hidasta.
Tämä on hyödyllistä kitkaa. Terveydenhuollossa järjestelmän hitaus ärsyttää, mutta osa hitaudesta suojaa potilasta. Potilastietoja ei voi käsitellä samalla logiikalla kuin markkinoinnin kampanjadataa. Mallin virhe voi tarkoittaa väärää jatkohoitoa, turhaa huolta tai väärää turvallisuuden tunnetta.
Riskit eivät ole sivuhuomio
Väärä vastaus on terveydenhuollon AI:n näkyvin ongelma. Vaarallisempi asia on väärä vastaus, joka kuulostaa varmalta ja tulee keskelle kiireistä työnkulkua.
WHO:n vuoden 2024 ohjeistus suurille multimodaalisille malleille nosti esiin viisi käyttötapaa: diagnoosi ja kliininen hoito, potilaan ohjattu käyttö, hallinnolliset tehtävät, lääketieteen koulutus sekä tutkimus ja lääkekehitys. Samalla WHO varoitti vääristä, puutteellisista ja vinoutuneista vastauksista, automaatiovinoumasta ja kyberturvariskeistä.
Automaatiovinouma on tässä yksi tärkeimmistä sanoista. Se tarkoittaa, että ihminen alkaa luottaa järjestelmään liikaa, koska vastaus näyttää tekniseltä, täsmälliseltä ja objektiiviselta.
JAMA Network Openin analyysi tekee tämän konkreettiseksi. Vuoden 2024 elokuuhun mennessä FDA:n listalla olleista 903 AI-laitteesta kliininen suorituskykytutkimus oli raportoitu 505 tapauksessa. Prospektiivisia tutkimuksia oli 41. Satunnaistettuja tutkimuksia oli 12.
Lisäksi ikä- ja sukupuolikohtainen suorituskyky jäi usein raportoimatta. Sukupuoliryhmien tiedot olivat saatavilla alle kolmasosassa niistä laitteista, joilla oli kliininen arviointi. Ikäryhmittäiset tiedot löytyivät vielä harvemmin.

Tämä ei tarkoita, että laitteet ovat huonoja. Se tarkoittaa, että julkinen tieto niiden yleistettävyydestä on usein puutteellista. Malli voi toimia hyvin yhdessä sairaalassa ja heikommin toisessa, jos kuvantamislaitteet, potilasjoukko, kieli, hoitokäytännöt tai datan laatu eroavat.
Terveydenhuollossa benchmark ei riitä. Mallin pitää toimia siinä arjessa, jossa sitä käytetään.
Sama koskee vääriä positiivisia ja vääriä negatiivisia. Väärä positiivinen tarkoittaa, että AI näkee riskin siellä, missä sitä ei ole. Väärä negatiivinen tarkoittaa, että AI ei nosta esiin riskiä, joka olisi pitänyt huomata. Molemmat ovat ongelmia, mutta eri tavalla. Ensimmäinen voi täyttää järjestelmän turhilla jatkotutkimuksilla. Toinen voi antaa ihmiselle petollisen rauhan.
Siksi "kuinka tarkka malli on" on vasta pintakysymys. Pitäisi kysyä myös, missä potilasryhmässä tarkkuus mitattiin, kuka tarkistaa tuloksen, miten poikkeamat käsitellään ja mitä mittaria pidetään onnistumisena.
Mitä tämä tarkoittaa Suomelle
Suomella on tähän asetelmaan hyvät lähtökohdat ja tutut esteet.
Hyvä lähtökohta on data, terveysteknologia ja julkisen terveydenhuollon vahva rakenne. Suomessa potilastieto on laajasti digitalisoitua, ja terveysteknologiayrityksiä on paljon. FCAI on jo pitkään nostanut AI for health -teeman yhdeksi tutkimusalueeksi, ja Varhan CAIDX-hanke rakentaa käytäntöjä kliinisten AI-diagnostiikkatyökalujen testaamiseen ja käyttöönottoon.
AI Finlandin vuoden 2026 katsaus kuvaa samaa kenttää käytännön kautta: automaattinen kirjaaminen, kuva-analyysi, diagnostiikan tuki, lääkitysturvallisuus ja riskien tunnistaminen ovat kaikki alueita, joilla AI-tuotteille syntyy kysyntää. DigiFinlandin koordinoima kansallinen SOTE-tekoälyn ekosysteemi kokoaa raportin mukaan yli 260 organisaatiota.
Esteet ovat yhtä tuttuja. Tietosuoja, hankinnat, järjestelmäintegraatiot, vastuunjako ja sääntely hidastavat käyttöönottoa.
Suomessa hyvä ensimmäinen askel ei välttämättä ole rohkein diagnoosimalli. Se voi olla potilaskirjaamisen, lausuntoluonnosten ja hoitosuunnitelmien päivitysten kaltaista työtä. Niissä riski on rajatumpi, hyöty näkyy nopeasti ja ammattilainen säilyttää luonnollisen tarkistusroolin.
Tätä ei kannata vähätellä. Jos malli säästää lääkäriltä muutaman minuutin jokaisella käynnillä, vaikutus kertautuu tuhansissa vastaanotoissa. Jos se vielä tekee tekstistä potilaalle ymmärrettävämpää, hyöty näkyy tehokkuutena ja parempana hoidon jatkuvuutena.
EU:n AI Act tuo terveydenhuollon AI:lle lisää kehikkoa. Komission FAQ:n mukaan AI-pohjainen lääketieteellinen ohjelmisto voi luokitella korkean riskin järjestelmäksi, jos se on osa säänneltyä tuotetta tai täyttää korkean riskin käyttötarkoituksen ehdot. Useille säänneltyihin tuotteisiin upotetuille korkean riskin järjestelmille velvoitteet alkavat 2.8.2027. Osa muista AI Actin säännöistä tulee sovellettavaksi jo aiemmin.
Tämä on hidas tie. Mutta se voi olla myös järkevä tie.
Suomi voi erottua luotettavalla käyttöönotolla. Oikea potilasryhmä. Hyvä data. Ammattilainen päätöksentekijänä. Selkeä vastuu. Seuranta käyttöönoton jälkeen.
Jos nämä toteutuvat, AI voi keventää terveydenhuollon painetta ilman, että potilasturvallisuudesta tehdään kokeilukenttää.
Mihin kannattaa kiinnittää huomiota
Kun seuraava terveydenhuollon AI-uutinen tulee vastaan, älä kysy ensimmäiseksi, onko malli "parempi kuin lääkäri". Se on usein huono kysymys.
Paremmat kysymykset ovat käytännöllisempiä.
Onko käyttötapa rajattu vai yritetäänkö AI:lla ratkaista koko hoitopolku kerralla?
Käyttääkö malli dataa, jota terveydenhuollossa syntyy jo valmiiksi?
Onko ihminen aidosti päätöksentekijä vai muodollinen kumileimasin?
Onko mallia testattu samankaltaisessa potilasjoukossa kuin missä sitä aiotaan käyttää?
Mitä tapahtuu väärälle positiiviselle ja väärälle negatiiviselle?
Mitataanko hyötyä potilaan lopputuloksissa vai vain työnkulun nopeutena?
Hyvä terveydenhuollon AI kuulostaa harvoin itsenäisimmältä. Sen vahvuus on siinä, että virheet voidaan löytää ajoissa.
Lääkäri pysyy vastuussa
Terveydenhuollon AI:n kiinnostavin muutos on hiljainen: kone lukee kuvia, tiivistää käyntejä, etsii riskisignaaleja ja auttaa tutkijaa kysymään parempia kysymyksiä.
REDMOD ja Virtual Biology Initiative ovat tästä saman suunnan kaksi ääripäätä. Toinen katsoo yksittäistä potilasta. Toinen yrittää mallintaa solua.
Välissä on suomalaisen terveydenhuollon arki. Ja siellä ratkaisevat lopulta samat asiat kuin ennenkin: vastuu, näyttö ja luottamus.
Siksi terveydenhuollon AI:ta kannattaa arvioida vähemmän demojen ja enemmän käyttötilanteen kautta. Sama malli voi olla hyödyllinen rajatussa työnkulussa ja vaarallinen väärässä paikassa. Luotettava käyttöönotto syntyy vasta, kun ammattilainen ymmärtää, mitä malli osaa, missä se epäonnistuu ja milloin sen ehdotus pitää ohittaa.
Tämä on terveydenhuollon AI:n arkinen lupaus. Vähemmän mystiikkaa. Enemmän näkyviä apukäsiä niihin kohtiin, joissa järjestelmä on jo valmiiksi kuormittunut.
Lähteet: Mayo Clinic News Network, Gut / BMJ, Biohub Virtual Biology Initiative, FDA AI-Enabled Medical Devices, JAMA Network Open, WHO, European Commission: AI Act FAQ, Sitra, FCAI, Varha CAIDX, AI Finland 2026
Haluatko sparrailla AI:sta etäkahvitellen?
Tekoäly voi olla voimakas työkalu, ja näiden aloittelijaystävällisten vaihtoehtojen avulla voit hyödyntää sitä omissa projekteissasi – olipa kyseessä sisällöntuotanto, ohjelmointi, markkinointi tai oppiminen.
Jos kaipaat koulutusta tekoäly-työkalujen käyttöön, nappaa tästä sitoumukseton etäkahvitteluaika ja jutellaan tarpeistasi 👇